点评 | 赵国屏(中国科学院院士)、陈芬儿(中国工程院院士)
微生物药物在“绿色智能制造”的整个过程中面临着诸多卡脖子问题,比如,如何建立新策略实现高效、绿色、智能的产量提升?链霉菌以能够生产大量的次级代谢产物而著称,这些产物正是微生物药物的重要来源。然而,链霉菌在长期的进化中获得合成次级代谢产物的能力,只是为了更好的生存(如与其它微生物竞争营养物质等资源),并不是生来就是人们理想的“药物生产工厂”。因此,要实现链霉菌为人类所用的目标,就必须深入解析影响这些代谢产物产生的共性规律,进而在认知的基础上改造链霉菌代谢途径,获得高效链霉菌微生物细胞工厂,从“格物致知”,到“建物致知”,再到“建物致用”。
聚酮类药物是链霉菌产生的一类重要次级代谢产物,其生物合成过程受到严谨的控制,只有在菌体生长进入稳定期才大量合成。稳定期由于营养限制,菌体物质不再快速合成,胞内初级代谢产物浓度显著降低,但聚酮类次级代谢产物开始大量合成。然而聚酮合成的前体是初级代谢的中间代谢物,此时浓度降低的这些中间代谢物如何满足聚酮大量合成的实际需求? 胞内代谢流从以初级代谢为主转换到次级代谢大幅上升,其中调控的扳机点是什么?另外,除了直接来自初级代谢途径,是否还有其它胞内代谢途径也参与并贡献了聚酮合成?我们又如何理性的精准控制这些相关代谢途径,使聚酮类药物更高效的合成?
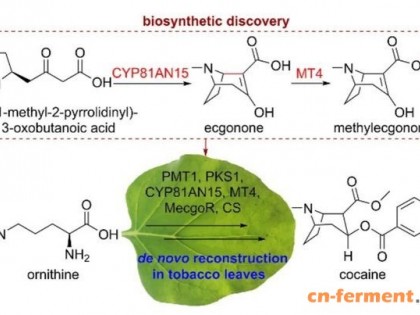
2019年12月9日,华东理工大学张立新教授联合中国科学院微生物研究所王为善研究员和中国农业科学院植物保护研究所向文胜教授在Nature Biotechnology杂志上发表文章Harnessing the intracellular triacylglycerols for titer improvement of polyketides in Streptomyces,在长期对链霉菌聚酮类药物生物制造研究的基础上,针对上述一系列未解之谜进行了深入探索(图1a)。该工作被审稿人评价为:“这是70年来首次在代谢水平上清晰阐明链霉菌初级代谢到次级代谢的代谢转换机制并进行工程应用”。 

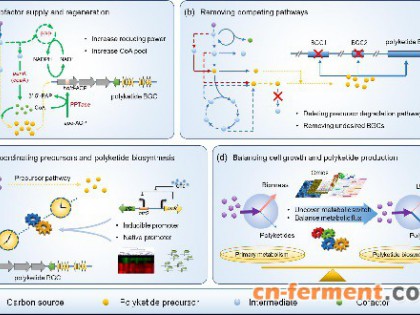
图1:链霉菌内源三酰甘油(TAG)在衔接初级代谢和次级代谢、调节代谢转换中的关键作用(a);基于调控TAG建立的次级代谢产物高产策略(b)。


据了解,该论文经过历时一年半的投稿,最终于2019年12月09号在Nat. Biotechnol.杂志(DOI:10.1038/s41587-019-0335-4)以长篇论文 (article)形式在线发表。审稿人评价道:这是70年来首次在代谢水平上清晰阐明链霉菌初级代谢到次级代谢的代谢转换机制并进行工程应用(This is a fascinating discovery. To my knowledge this link has never beenestablished in the 70 years since the use of polyketides as antibiotics andother drugs began……)。无独有偶,与张立新教授团队发现的链霉菌代谢转换机制类似,美国HalAlper教授也在metab. Eng.杂志上同时发表文章(DOI:10.1016/j.ymben.2019.11.006),报道了在真菌系统--解脂耶氏酵母菌中控制内源TAGs的降解能够有效提高III型聚酮类代谢产物的产量。

图2:阿维菌素产学研国际联盟启动仪式(a),挂牌(b)。
赵国屏(中国科学院院士,中国科学院合成生物学重点实验室主任,合成生物学专家)
陈芬儿(中国工程院院士、复旦大学化学系教授,精细有机化工和原料药制造专家)
https://www.nature.com/articles/s41587-019-0335-4