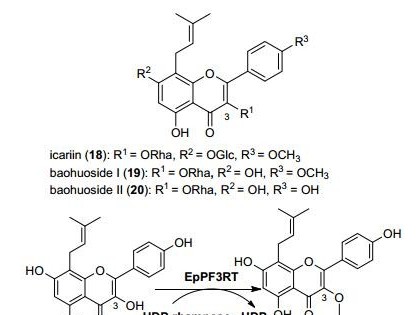
前言
饲料业和养殖业在快速转入了平缓期的情况下,发展面临的焦点问题已经由利润变为生存、饲料产量变为质量、变为直接消费的畜产品质量问题。畜禽养殖更是全行业同时面对WTO和日益加大的禁用抗生素的压力,提前进入平均利润期。在这样的背景下,从管理添加剂入手,及早剔除有害物;从质量入手,确保质量和使用效果是缓解当前世界范围内养殖业承受安全压力的有效措施。众多的饲料厂、中小城市养殖企业(户)再不可还憧憬滥用违禁药物、非法添加剂和搀杂使假的喜悦之中,及早依靠合法、安全、有效的产品及技术才是降低成本,提高生产性能,增加产品竞争力的唯一途径。植酸酶在几年内就成为一个广受欢迎、大面积应用的饲料添加剂,在全球范围获得环保和经济双重效益。在我国已经覆盖了相当大范围的产蛋鸡饲料,在猪饲料中的应用也上升很快。但与此同时,一些相关的法规或措施亟需同期配合。着无论对保证用户的利益还是保证饲料的质量必不可少。如商品植酸酶及饲料产品中含量的测定方法、饲料中添加了植酸酶以后总磷水平的改变如何在执行的饲料产品质量标准中反映出来等等。这些问题不解决,将无益于饲料质量的改善和保护用户的利益,更有碍于植酸酶的进一步发展。本文将根据掌握的有关部门资料,讨论和分析测定植酸酶含量的必要性极其测定方法,特别是集中评价差异的部分。使各类不同的企业和机构能按照各自的目的和要求提前做好准备,避免在选择方法和添置设备室造成浪费。充分利用分析测定手段,保障各方面的权益。
商品植酸酶的质量是使用效果的基本保障
随着植酸酶的大规模应用和展现出的经济效益,商品植酸酶本身的质量成为加酶饲料 及其动物性能的首要保障,随后才是应用技术。植酸酶与其它酶制剂同样面临的特殊问题是含量测定。植酸酶的含量在不同商品间可以差一个数量级以上;高温和常温极其在高浓度预混合饲料中酶的损失直接影响保值期和使用的效果;含量直接决定了添加量的高低,直接影响使用者的开支成本。另外,企业对加酶饲料产品的质量管理控制集中到酶含量方面。分析检测能力不高的众多中小企业面临如何选择和鉴别植酸酶产品的问题。这些都已经成为使用者的当务之急。在众多影响使用效果的因素中,产品本身的原因主要包括酶的种源、含量、温度稳定性、容重、pH特性及体内水解效率等。可以人为酶活性含量是最重要的质量指标。因此无论在植酸酶的制造、贸易、应用甚至纠纷仲裁、以及加酶饲料的质量控制和检测都亟需统一、标准的含量测定方法。这不仅四海开展几乎全部与质量有关部门的工作的必要手段,也是植酸酶发挥效果的基本前提。
权威的活性定义是制定规范方法和保证质量的基本前提
由于酶的特殊性,当面临不同酶系种源、不同产品规格、不同用途时,统一、标准的测定方法就自然成为进行几乎所有工作的前提。是否有一种方法可以测定各种不同来源的植酸酶?BASF-DSM回答了这个问题。标准方法与企业,大学或研究机构的方法在要求和用途上完全不同,覆盖的范围和准确度和精密度也不完全一样。
讨论测定植酸酶含量的标准方法之前,活性单位的定义自然成为首要工作。可以设想,如果没有合理、严格、一致和公认的定义,各方面都利用对自身方便的有利条件定义植酸酶的活性单位,则必然陷于混乱和无休止的争论。造成根本无法鉴别的比较的状况。其实这样的例子在添加剂领域并不鲜见,特别是新产品出现的更多。所以必须首先制定和明确[植酸酶活性单位]的统一定义。源自酶本身的特殊性,酶活性的定义比其它定义复杂。含量的测定和表示区别于其他饲料成分,不能直接测定酶自身的含量,不是以酶自身物质或其对应的蛋白质组分为测定对象,也不能以质量或%表示,无法用阿拉伯数字后接一个物理量词(如5公斤,20秒等)的规范命名原则表示活性。至今为止国内外的法定机构尚未对[酶活性单位]制定统一的定义,仍多沿用国际生化联合会酶学委员会的建议(陈茂彬,2000)。既1酶活性单位是指在规定的条件下,每分钟转化1微摩尔底物所需要的酶的数量,除了建议的温度(25℃)以外,包括pH、缓冲液、底物的浓度均采样[最适宜条件]。既以在特定的条件下测定反映产物的数量变化作为表述对象。通常沿用酶的名称加[活性单位]共同表示活性的高低。其它酶制剂应用领域也采用类似的表示方法。而这样定义得出的酶单位变化完全依赖于上述反映的条件且极为敏感,任何一个因素的微小改变,则导致结果差之千里。明确标注出反映条件就是定义活性单位的实质工作。
目前在世界上最多用FTU(Fytase Unit的缩写)表示植酸酶活性单位。Fytase是荷兰文植酸酶。最先早于BASF-GB公司提出并使用。1植酸酶单位定义:在37℃和pH=5.5的条件下,每分钟从浓度为0.0051摩尔/升的植酸钠溶液中释放出1摩尔无机磷所需要的植酸酶的数量。1994年该定义及文字缩写被AOAC在推荐方法中被直接引用,作为统一的标准使用Journalof AOA Cintenational Vo1.77.No.3,760-764)。自此定义工作实际上已经完成,被包括我国在内的国际质量认定机构、权威检测机构、仲裁机构普遍接受和采用。食用化学品法典(FCC-Food Chemicals Codx.IV.1996.p808-810)和VDLUFA(VDLUFA-Methodenbuch Band III,4.Erg.1997)极其相当多的研究报告也都是直接使用FTU表示植酸酶的活性(植酸酶实用指南,张若寒,2001)。在我国刚制定的国家标准中也采纳了同样的定义,是目前国标中与国际先进标准接轨不多见的范例。。植酸酶工业产品的质量规范也采用了这一定义。有了统一的酶活性定义,就等于有了一把统一的尺子,为植酸酶活性的定量标准化工作奠定了基础。
在三重情况下可能见到不同的植酸酶活性单位。首先是定义的内容完全不同,仅使用了不同文字的缩写表示,如使用FTY的Novo Nordisk公司;其次则是定义的关键测定条件(37℃,pH=5.5)、反应底物(正植酸钠)及其浓度(0.0051摩尔/升)都与标准定义的对应内容一致,而差别只是在度量时间(小时,分钟或秒)和水解产物量的表达方面( mol(10-6mol)—微摩尔浓度,nmol(10 mol)—毫微摩尔浓度或毫克)。所以,这也仅是一个简单换算问题;最后一种情况是完全改变了定义的关键测定条件,例如据rohm公司介绍,其使用的PPU定义是将pH规定在6.0。以这样定义表达的植酸酶活性含量完全失去与标准定义下的数值的直接可比性。
在涉及质量和研究的报告中,后两种情况并不多见。尚未见到对其进行的研究报告和应用实例,故硬性规定不大。唯一在实际中需要提防的是仅仅利用定义中[植酸酶单位]这一相同的文字名称,而以不同的表达单位将低含量的产品活性表高的可能性,造成对用户的误导。
在一些刊物或非正式印刷品中出现过用[国际单位]作为植酸酶的活性单位使用,也是不规范、不正确。国际单位—IU源自International Unit的缩写。在动物营养领域,IU至今尚仅作为维生素A和D3的法定活性单位,而且有其历史原因。在我国,按照国家标准中对饲料工业通用数语的规定,IU也仅限定于表示维生素活性的计量单位。况且至今并未有任何国际组织宣布将现行的植酸酶活性单位定义作为国际单位使用。所以不宜擅自在植酸酶活性单位前加[??闿二字。
第二步就是要制定出反映专一性的测定程序。如果没有标准、一致的测定方法,其危害是导致同一样品得出的不同结果,或者数据大精度不同,平均值的置信区间不同等一系列问题。危害不比定义混乱小,不同数据掩盖在相同的[定义]下,使用这样的数据,一般人辨别不了,还可能导致分析设备的配置错误。与定义相比,测定程序的标准化相对比较容易。或者可以简单地理解为将定义的具体实施步骤固定下来。其核心是精度。虽然测定程序的标准化工作包括了规定精度,试剂,标准对照品,水解底物,空白设置,酶及其它试剂添加顺序,培养温度和时间及其控制等各项内容,但是以最后二项至为关键。
标准方法的进展现状和用途
如上所述,目前植酸酶单位的定义已经获得了统一的共识,而规范测定方法程序方面也已经完成了大部分的工作。其形成过程大致如下:
·1991年巴斯夫和Gist-Brocades在确认了植酸酶含量单位定义的同时,向外界公开了企业使用的测定植酸酶含量方法的荷兰文版。当时使用的方法既现在所说的绝对法。主要是用于植酸酶生产企业的内控和欧盟饲料添加剂的管理和审批机构作为检测手段;
·1993年以后随着在世界范围内包括用户和其它制造商在内的各方面经过不断的使用、比较、筛选和修订完善,形成了绝对法和相对法,继而出现将二者合一的两步法。[两步法]是绝对法和相对法联用测定步骤的简称;
·1994年在相对法得到普遍认可的前提下成为世界上权威的AOAC推荐该方法作为测定饲料中植酸酶的标准方法(Phytase Activity in Feed Samples Usinga Colorimetric Enzymatic Method,I-26);
·1996年FCC批准相对法作为食品中植树酸酶含量的常规分析方法;
·1997年德国(VDLUFA)将两步法规定为饲料中植酸酶含量的国家级标准分析方法。
·2000年我国的科学工作者在全面研究和论证了要求和使用对象范围以后,选择了「两步法」作为制定推荐性国家标准的基础。全部技术和文本的起草以及终审工作于2000年底完成,待政府有关部门的最后批准和发布。与AOAC的方法比较,可以讲达到了世界先进水平。实现了一步到位,与国际先进方法接轨的目的。同时有适合国情的独到之处。
至此,国际质量认证及仲裁机构和世界各国均认可和接受使用该方法获得的测定结果。目前仍在进行的工作报告AOAC将其由推荐性标准方法升级为官方标准测定方法。AOAC复验批准发布酶的官方标准测定方法程序非常严格,要经过三个主要步骤:
·在2000年5月将已经获得官方方法委员会初审通过的推荐方法与其应用协作研究报告一同于2001年上半年在AOACinternational杂志的纲要中公布,在AOAC(17th,2000)执行;
·获得最后终审批准资格是自该方法作为推荐方法起2年内委员会未收到任何实质性质疑的条件下,由终审委员会(GeneralReferee)和分析方法委员会以投票决定提交终审;
·终审由官方方法委员会将终审方法提交有投票权的AOAC委员,以投票决定终审结果。
由此可见,标准方法的诞生并非由某人或某机构指定而出,有一个相当长和科学论证过程。以当前的进展看,AOAC的推荐方法将作为标准方法使用的方向逐渐清晰。权威机构标定植酸酶标准对照品使用绝对法,其它用户向使用相对法方向靠拢。
绝对法和相对法的测定流程、主要差别和对设备的要求

绝对法和相对法的测定流程示意图如上:
顾名思义,绝对法是不借助中间物质和步骤,直接使用定入中的无机磷作为衡量释放无机磷精选量的工作标准曲缍,测定植酸酶含量。但是方法本身先天的因素造成测定精度低。为了保证准确度,必须加大测定的重复数,靠取平均数的办法获得可靠的测定值。所需时间长,费用高。绝对法适用于法定的质量认证及促载机构标定植酸酶标准品含量,为一般单位常规提供基准物质。相对法是借助已知准确含量的植酸酶标准对照品作为工作标准曲线,间接获得样品的植酸酶含量。其测定结果精度高,速度快,费用低。高精确度是通过延长培养时间和利用等测定条件的误差低消来达到的。适用于一般有日常测定需要的机构、企业使用。由于精度高,减少了重复次数,可以增加同一测定批次的样品数。两种方法的根本区别就在于对照品不同。分析来自不同实验室的测定结果(见表达1—3),无论以CV%或s表示的精确度都有近几3来倍的差异。
| 表1.绝对法和相对法的变异系数(CV%) | ||
| 绝对法 | 相对法 | |
| 相酸酶产品 | 2.5-4.9 | 0.9-1.5 |
| 加酶饲料 | 5.8 | 1.9-2.0 |
| 加酶预混料 | 4.0 | 1.7 |
| 表2.绝对法测定的标准差(s%) | |||
| 实验室1 | 实验室2 | 实验室3 | |
| 稀释间 | 0.1 | 0.5 | 1.4 |
| 称重间 | - | 0.7 | 0.5 |
| 底物间 | 0.5 | 0.8 | 0.4 |
| 日间 | 1.6 | - | 0.2 |
| 总体误差平均值 | 0.94 | 0.41 | 0.37 |
| 平均值和90%置信区间(FTU/g) | 46660±1280 45380-47940 |
47090±450 46640-47540 |
46100±500 45600-46600 |
| 表3.相对法的变异系数(CV%) | ||
| 实验室内 | 实验室间 | |
| 植酸酶产品 * | < 2.5 | < 5.0 |
| 加酶饲料和预混料 ** | 5-10 | 10-15 |
* 适用于各种类型和含量浓度的植酸酶产品;
** 适用于添加不同水平植酸酶的各种类型饲料和预混料制成品。
以一个高水平仲裁实验室在及其严格控制的实测结果为例可以清楚地观察到精度的差异:分别使用绝对法和相对清测定同一添加了植酸酶的模拟饲料样品(300FTU/公斤饲料),绝对法的相对偏差为7·6%,造成的绝对误差为23FTU,测定结果为288-312FTU;而相对法为2.7%,在饲料中导致的绝对误差为8FTU,测定结果为296-304FTU。再以含量为5000FTU的商品植酸酶为例,绝对法的相对偏差为5%,造成的绝对误差为250FTU,测定结果为4875-5125FTU;而相对法仅为1.8%,导致的绝对误差公为90FTU,测定结果为4955-5045FTU。可以说,以上的误差是方法的误差,无法利用方法内的其它措施补救。因此,试图通过提高测定第件和环境的控制程度将绝对的精度改善至相对法的水平没有意义。这同样不是操作人员的技术水平问题。就饲料企业的实验室测定精度而言,出现更大的误差并不意外。
最相想的测定方法是准确度和精密兼任,但实际上很难找到。所以,优秀的酶测定方法首先要具备在有限的重复测定次数间有良好的精度,其重要性在准确度之先。利用高精度数据进行系统误差校正就能获得目标植。相反则只有加大测定的重复次数。
如果使用绝对法测?ㄋ橇涎?吩蛐枰?赋龅氖牵??诰?苑ㄎ?乐钩鱿治蟛猓?ㄒ榱嗽錾琛癉oublecheck"的要求,既用无机磷作为计算结果的标准曲线,不能省却用已知含量的值酸酶对照品的附加「标准对照品复验」步骤。
一个需要回答的问题是为什么需要两种方法呢?既然绝对法的测定值准确,是相对法的测定基础,又为国际,国内的法定和仲载机构认可,何必再多一个相对法?问题在于绝对法复杂耗时,重复数量大,设备要求高,开支大。这对于一般以常规质量控制为测定目的的企业用户来讲绝非小事,也是不少企业对分析化验和而不为的重要的原因之一。同样,既然相对法利用植酸酶标准对照品保证了测定值的准确性,只需设置较少的重复数即可获得很高的精度,费用低,又何必再多一个绝对法?问题是没有绝对法,植酸酶标准对照品的精度含量从何而来?所以理想的解决方案就是将两者结合起来,形成「两步法」。
两步法的适用对象、可能面临的难点、解决方法和注意事项
·相比之下,「两步法」综合了绝对和相对法各自的优势,克服了局限
,其优点集中在以下几个方面:
·配套方法的适用范围覆盖了几乎所有各类含酸酶的样品,能满足从大量标定植酸酶标准对照品到测定各样品中植酸酶含量的所有要求;
·绝对法用于法定的质量认证及仲载机构标定植酸酶标准品含量,为常规测定提供基准物质。既摆脱了以往完全依赖国外供应造成的标准对照品来源限制的局面,也某种程度上在质量纠纷仲载和监控中体现出国家的主权;
·相对法则用于日常测定工作。既有绝对法的权威准确度,又有相对法的高精度和简单快速的特点。企业不必配置昂贵的专用设备,对操作人员无特殊要求。不一般实验室条件下精度都可达到表3的水平。测定速度能够达到20独立样品/人,日;
·国际质量认证及仲载机构和世界各国均认可和接受该方法的测定结果。
使用两步法可能会遇到以下问题,对应的解决方法如下:
·饲料要有代表性样品,要粉碎,否则CV超过20%。称样量可以增加到100克,100ml提取,可以降低CV,但很不方便,浪费试剂。酶样品一定要充分溶解,对保证准确测定难溶样品中的酶含量至关重要;
·不同的样品不能使用同一种缓冲液TitriplexIII(EDTA)用于矿物质预混料;高剂量氯化钙用于降低配合饲料的背景干扰,改善因高含量磷导致低的低回收率,扩展回归曲线的有效工作范围;Tween20用于防止酶蛋白附著在玻璃器皿上;牛血清蛋白(BSA)是植酸酶的稳定剂,还能防止酶蛋白在玻璃器皿表面附著;
·每一试管的开始培养时间要有精确的、固定的、足够的(完成下一步骤所需要的时间)时间间隔,以保证精确的结果,否则CV上升;
·所有影响酶反应的因素都必须精确控制才能保证绝对法的精度,包括温度,培养时间,缓冲液浓度和pH值。不同测定日的差异增大,必须天天独立控制。相对法却可以在不丧失精度和准确度的前提下容许以上因素的微小差异而增加速度;
·相对法的培养时间为60分钟。某些样品中酶反应达到平衡需要的时间不同,特别是后保护的产品,含有可能影响酶释放速度的辅料,为了覆盖所有情况,60分钟是安全的。对一些内源酶,需要更长的时间才可以使酶反应平稳。降低水解反应曲线的斜率。对于酶活性释放速度低的产品有利;
·对精度有要求的设备包括天平,取样器,计时器和恒温培养箱。对天平的要求是由于称取标准品的需要。绝对法一定要配备高精度的自动取样器或使用高精度的移液管(大肚吸管)代替刻度吸管,而相对法的要求则比较低。对恒温培养箱的精度要求为箱内不同部位容许的温差。绝对法为37℃±0.1℃,显著高于相对法的37℃±0.5℃(0.2-0.5)。如果企业经费条件限制,无高精度恒温培养箱,可以自增内循环搅拌器以达到要求;
·高精度读数的计时器对绝对法和相对法都是必需的;
·离心的时间和速度是可以改变的,10-20分钟,2500-4000rpm;
·无机磷曲线呈完全直线,酶曲线为二次曲线。无机磷曲线无法反映出酶反应的对数剂量特性;
·必须正确储存和使用标准对照品。低温冷冻(-40℃)存放,每包装单位一次性开启即用,不能重复冷冻存放;
·全部测定过程中必须使用无磷水、无磷洗涤剂和无蛋白吸附的器皿。
两步法作为国家级的完整配套测定实施方案,绝对法和相对法分别适用于不同的目的。绝对法适用于国际和国家的法定或授权的仲载机构标定标准对照品使用。在科学研究或产品开发中,面对完全不了解特性的新酶来源,可以考虑先使用??苑ǔ醪矫?髌浠钚院?亢吞卣鳌N?Vげ舛ǖ木?范龋?甓ㄒ桓鲅?沸枰?辽儆?3个认证实验室参加。每个实验室测定24个数据。既植酸酶的活性要在3个工作日来测定,每天用待测植酸酶测定两个植酸钠底物样品,每个植酸???飞杵叫胁舛ǎ?扛銎叫胁舛ㄉ枰桓鲋馗矗╪=24,3x2x2x2)。用于在国内使用的植酸酶的标准对照品应考虑在获得国家权威质量监督部门授权的国家级实验室间进行重复测定;如果是在国际范围使用,则要在不同国家的认可实验室间进行。在重大的仲载案件中,如果直接使用绝对法,如前所述,仍然需要用标准对照品复验;相对法适用于除了标定标准对照品以外的各种测定。
只要能确保使用的标准对照品标量准确无误,储存恰当,就完全能达到准确、快速和经济的目的。
尽管选用「两步法」中的相对法已经很简单,但对于分析检测能力不高的小型企业,或从控制成本的角度考虑,可以继续使用供应商质量承诺的方法(植酸酶实用指南,张若寒2001),仍然不失为明智的选择。
植酸酶活性含量测定的特殊性
包括两步法的全部测定结果在内,都是植酸酶在体外的活性值,不能反映体内效率的差异。即存在著测定的活性含量一样,而使用性能不同的可能性。这是一个目前尚示解决的问题。植酸酶含量是在体外测定的,能否在动物体内发挥出同样的作用是另外一个问题,植酸酶的种源差别目前主要集中在微生物种源的3-phytase和植物种源的6-phytase之间。差异表现在不同的pH值特性和对植酸的水解效率。酶的体外测定值与实际发挥作用的条件,即在动物体内发挥作用时的情况不同。在某种程度上可以将体外测定值理解为最大值,而且很难在体内重现最大值效应。这与其它化学类营养物质的测定一样,是在体外进行,与体内的代谢有差别。如AA,测定的是总量而不是可利用量。不能强求植酸酶成为例外。所以在应用测定值时,要给予注意。如果企业利用测定值推长时期诸如添加量等与单位体内反应直接相关的数据更要特别注意。
摘要
由于酶制剂活性定量分析的复杂性和难度,制定含量测定程序的前提是酶活性单位的定义;而测定程序标准化的前提是定久的标准化。酶活性对反应条件十分敏感,测定条件和不同的测定程序对结果有极大影响。标准化的测定方法并非公为监测部门使用的工具,也能为使用者带来保障和很大好处。通过了解两步法和逐步演变成AOAC标准方法的过程、原则,不仅有助了解植酸酶测定方法国际化和标准化的现状,也帮助使用者正确地选择适合的方法和必备的设备。对容易忽视的测定技术细节和难点的分析则可能使初用者少走弯路和避免了易犯的错误。现有的植酸酶活性测定技术仅提供了在体外评价商品植酸酶质量的保证方法。并不适合用于反映植酸酶在动物体内的活性,也无法完全反映出具有不同生物利用活性或不同来源的植酸酶在生物体内的差异。植酸酶的测定方法虽然有限,时间也不长。相信会在不断的应用中不断地进步。
参考文献(略)
(此文为待发表稿请勿转载)
作者简介:
张若寒 ,男。1956年3月6日出生。1981,84和92年获学士,硕士和博士学位。现任职巴斯夫公司负责营养型饲料添加剂的应用技术研究、产品开发推广、质量和技术咨询。兼任农业部饲料工业中心客座教授。主要从事的研究领域涉及单胃动物氨基酸营养,饲料成分分析,非常规饲料原料资源开发研究及饲料、饲料添加剂和食品添加剂的国家质量标准的制定工作。