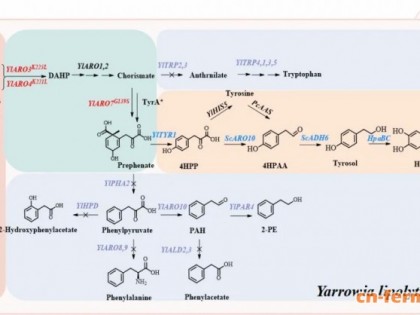
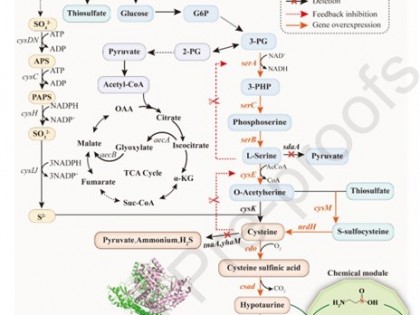
强心苷甾体是广泛分布于自然界的一类特殊的代谢产物家族,其结构的甾体骨架中往往含有一个特征的C14β-OH,C17位由五元或六元不饱和内酯环连接(代表了两类强心苷结构类型),同时C3位可能存在糖单元修饰。植物产生的强心苷分子往往C17位包含有一个γ-丁内酯环;而两栖动物,如蟾蜍中产生的强心苷C17位则为δ-戊内酯单元(图1)。多年来该类分子主要用作强心剂,随着强心苷分子的抗肿瘤、抗炎、抗病毒等活性的开发,丰富且良好的生物活性使其目前活跃于多项临床研究中。然而,目前工业生产该类药物仍然采取从动植物中原位提纯的方式,这严重限制了强心苷分子的应用;此外强心苷结构上的微小差异极大地影响了其生理活性。因此越来越多的研究致力于探索和解析强心苷复杂结构的生物和化学合成过程,为其更高效地工业量产提供新的思路。

图1 强心苷明星分子
2022年7月28日,ACS Catalysis期刊在线发表了戈惠明团队关于强心苷甾体的最新研究成果。通过生物催化甾体小分子雄烯二酮的C14位发生惰性C-H键的活化,再联合化学手段构造一条高效的合成途径,并成功运用于两类强心苷天然产物—bufotalin, bufogenin B, digitoxigenin的合成。

图2 生物和化学催化的强心苷分子的交叉合成策略
在前人的研究中,强心苷分子的生物合成主要集中于由胆固醇前体代谢形成孕酮等甾体中间体的过程,对于特征的C14位羟基化以及C17位的不饱和内酯环的组装鲜有报道。因此,研究者针对该类分子特征的C14β-OH的形成展开研究,对可能催化羟基化的P450酶进行挖掘。首先选取能够产生强心苷分子的植物牛角瓜为研究对象,对其不同组织的转录水平进行分析,最终通过筛选出候选的11个P450基因的功能验证,并结合强心苷生物合成中间体—孕酮和其结构类似物雄烯二酮的饲喂,确定了CYP11411能够催化甾体C14位产生α-OH,而该构型与目的构型相反。研究者对另一类强心苷产生宿主动物蟾蜍进行研究,发现CYP44476同样能够催化甾体小分子底物发生C14位的氧化羟基化,同时还能够催化甾体的C6、C9、C15位形成羟基。根据动植物宿主中羟化酶的研究结果,推测自然界可能优先通过直接攫取α-H产生α-OH,再经过脱水水合等途径完成构型的翻转。

图3植物牛角瓜及动物中华大蟾蜍的转录组分析、候选P450的功能验证及代谢产物的结构
该团队首次发现了强心苷产生宿主中的C14羟化酶,能够直接实现惰性甾体骨架的位点特异性氧化,而这通过化学反应则难以一步完成。为了完成强心苷分子的合成,研究者拟通过生物催化完成C14羟基化甾体的大量合成,再经过化学手段组装C17位的含氧杂环。因此,需要对C14羟基化甾体进行规模制备。通过对羟化酶的异源表达代谢谱分析发现其转化效率较低,于是通过将目标转至绿色高效地微生物生物转化。通过对微生物菌株的筛选和羟基化活性测试,最终发现新月弯孢霉C.lunata能够以较高效率催化生成目标产物(图4),进一步优化后分离收率能够达到70%,并获得了5g的C14α-OH-雄烯二酮。

图4微生物菌株的甾体C14位羟基化活性测试
接下来,研究者们着手于利用化学合成完成C17位五元或六元不饱和内酯环的组装。首先,通过底物C14α-OH-雄烯二酮的∆4,5位氢化还原构建A/B cis环系,然后选择性还原C3位羰基及羟基的硅醚保护获得化合物17。为了实现关键C14位羟基构型的翻转,先通过脱水消除α-OH,再经Mukaiyama水合产生β-OH产物。而在烯烃水化过程中,产物异构体比例与反应溶剂息息相关。由烯基碘中间体21出发,可分别偶联五元或六元内酯环(图5)。

图5 底物14α-OH-雄烯二酮合成关键烯基碘化物中间体21
为了完成强心苷甾体的合成,通过化合物21与锡试剂的Stiile 偶联反应构建了强心苷的基本骨架。∆16,17双键能够通过氧化形成三元氧环,经TMSOTf和2,6-lutidine催化形成C14硅醚而发生1,2-氢迁移实现开环重排。最终通过C16位羰基还原,乙酰化反应和保护基的脱除,成功获得了天然产物bufotalin和bufogenin B(图6)。

图6 天然产物bufotalin和bufogenin B的合成路线
由化合物21形成的烷基碘化物则更易发生自由基反应。化合物33与马来酸酐在自由基供体TTMSS和引发剂AIBN作用下完成类SN2自由基偶联反应。随后,在碱性条件下,生成的C14位羟基参与形成内酯环。NaBH4-MeOH选择性还原和内酯化(经历开环再成环过程)形成35,苯基氯化硒衍生物进一步氧化获得不饱和内酯环产物,酸水解后获得最终产物digotoxigenin(图7)。

图7 天然产物digotoxigenin的合成路线
综上,该团队首次从强心苷天然产生宿主中鉴定出两个能够催化C14位羟基化的P450酶——CYP11411和CYP44476,为其生物合成途径的阐释打下基础。同时通过微生物的高效转化规模化合成了甾体C14α-OH-雄烯二酮,并以其为底物通过组装不饱和内酯环单元完成了两类强心苷天然产物的合成。这种利用生物催化和合成化学的方式开发通用且灵活的合成策略,可用于创制更多生物活性的强心苷分子及其结构类似物。
南京大学生命科学学院赵阳博士生为文章的第一作者,南京大学生命科学学院戈惠明教授、谭仁祥教授和化学化工学院俞寿云教授为文章的通讯作者。该研究得到了国家重点研发计划、国家自然基金委杰出青年基金、青年基金及中央高校基本科研业务费等项目的资助。
原文链接:https://doi.org/10.1021/acscatal.2c02185