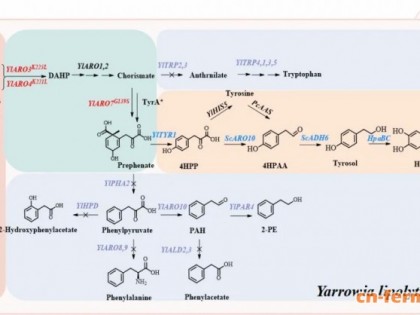
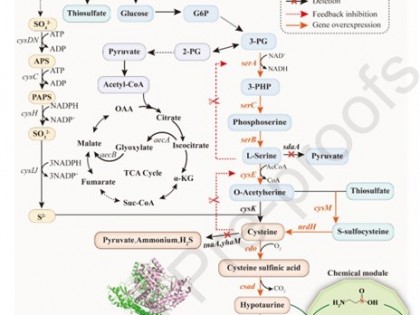
近日,湖南农业大学刘虎虎等人在《Biotechnology Advances》发表综述:A Review on Squalene Production by Engineered Yeasts: Current Advances and Perspectives。在合成途径方面,酵母主要通过胞质中的甲羟戊酸途径将乙酰辅酶A转化为角鲨烯,其中3-羟基-3-甲基戊二酰辅酶A还原酶、异戊烯基焦磷酸异构酶及角鲨烯合酶等关键酶的表达与活性调控对角鲨烯积累具有决定性作用。为提高滴度,有研究提出了多种策略:关键基因的过表达、角鲨烯下游代谢途径的削弱、细胞器区室化工程、辅因子工程以及角鲨烯外排的增强等。例如,通过过表达截短型HMG1基因与角鲨烯合酶ERG9,并抑制下游角鲨烯环氧酶ERG1,可显著提升角鲨烯的滴度;利用过氧化物酶体、线粒体或脂滴等细胞器进行途径区室化,不仅能提高局部底物浓度、减少副反应,还能有效缓解产物的细胞毒性。在前体(乙酰辅酶A)和辅因子(NADPH)的供应方面,有研究通过优化内源途径及引入外源模块(如PK-PTA途径)增强乙酰辅酶A供给;通过强化磷酸戊糖途径或表达NADPH再生酶提升还原力。此外,角鲨烯的胞外分泌策略通过表达转运蛋白(如Osh3、Pdr5)或融合分泌信号肽,有效减轻细胞内积累带来的代谢压力,并简化下游分离流程。

遗传工具的应用进一步加速了细胞工厂的构建。CRISPR-Cas系统能够实现精准的多基因编辑与调控;合成启动子工程使代谢通量得以精细控制;动态调控系统则能根据细胞生长阶段或代谢状态自主调整途径通量,实现生长与生产的平衡。除了常用的酿酒酵母和解脂耶氏酵母外,其他酵母物种如假丝酵母、毕赤酵母、圆红酵母等也展现出角鲨烯生产的潜力,尤其在利用廉价碳源和适应高密度发酵方面。未来研究需进一步结合系统生物学、深度学习与自动化平台,推动酵母平台的优化与放大。

总结而言,工程酵母生产角鲨烯已取得显著进展,最高产量已达克每升级别(55.8g/L)。然而,当前仍面临产量稳定性、生产成本及下游提取效率等多重挑战。未来的研究方向应聚焦于整合多维代谢工程策略、开发更智能的动态调控系统、挖掘新型酵母宿主,并推进从实验室到工业规模的发酵工艺优化与产物分离纯化技术升级。通过合成生物学、代谢工程与过程工程的深度融合,有望实现角鲨烯的绿色、高效、可持续生产,为相关产业提供稳定可靠的生物基原料。
(徐少元 摘译)