摘要概括
天麻素(Gastrodin)是传统药用植物天麻中富含的一种天然酚类糖苷,因其出色的抗氧化和细胞保护特性,作为高附加值化合物备受瞩目。然而,传统的植物提取法受限于自然丰度低、种植周期长等问题,而化学合成法则面临效率低和环境污染的挑战。近日,南京林业大学李迅团队在绿色化学与工程领域权威期刊 ACS Sustainable Chemistry & Engineering 上发表最新研究。该研究通过蛋白质工程与代谢工程的深度整合,在大肠杆菌中构建了一个高效、可持续的天麻素从头生物合成平台。通过对糖基转移酶AtUGT进行理性设计与组合突变,其催化效率大幅提升;同时重构了莽草酸途径和独立的UDP-葡萄糖(UDPG)再生途径,成功解除了前体供应瓶颈。最终,在1.1-L生物反应器中进行ink-id="link-1774409401988-0.4727608847584701">溶氧控制的补料分批碳发酵,天麻素产量达到了惊人的13.73 g/L,这是迄今为止报道的大肠杆菌中的最高产量。

研究背景
天麻素(4-羟基苯甲醇-4-O-β-D-吡喃葡萄糖苷)是医药和保健品领域的“明星分子”,广泛用于治疗中枢神经系统疾病及抗炎抗氧化。目前,商业化的天麻素主要依赖从植物天麻中提取,但这面临着得率极低(通常干重<0.7%)、占用大量耕地和自然资源消耗的困境。虽然化学合成可以作为替代方案,但步骤繁琐且不够绿色环保。
近年来,微生物细胞工厂(如酵母、大肠杆菌)为植物源天然产物的绿色制造提供了新思路。大肠杆菌因其生长速度快、遗传操作工具成熟,被视为理想的底盘细胞。然而,目前已报道的大肠杆菌ink-id="link-1774409401990-0.7972207047645055">合成天麻素的产量仍然较低(仅为毫克级),远达不到工业化生产的要求。如何打破代谢瓶颈、实现高滴度量产,是该领域亟待解决的难题。
研究问题
要在大肠杆菌中实现天麻素的高效量产,研究团队需要攻克以下四大核心科学问题:
- 酶的催化效率低:
如何挖掘并改造出具有高活性和高区域选择性的糖基转移酶(UGT),以高效完成天麻素合成的最后一步“糖基化”? - 芳香族前体供应不足:
如何引导更多的碳代谢流进入“莽草酸途径”,打破产物合成的物质限制? - 糖基供体(UDPG)匮乏:
天麻素合成需要消耗大量UDPG,如何能在不影响细胞正常生长(不与糖酵解争夺碳源)的前提下,实现UDPG的充足供应? - 发酵工艺放大:
如何在反应器放大过程中平衡细胞生物量与产物合成的关系,实现产量的最大化?
研究方案
针对上述问题,研究团队采取了“酶工程+途径重构+系统优化”的组合拳策略:
1. UGT酶的挖掘与蛋白质工程改造
团队首先对比了两种来源的糖基转移酶(AtUGT和RsUGT),发现拟南芥来源的AtUGT活性高出近10.5倍。随后,基于基于活性的序列保守性分析(ASCA)策略,对AtUGT的27个位点进行了定点突变。经过多轮组合,筛选出了一个性能卓越的三突变体 AtUGT (T282S/A294E/V463L)。为了揭示其活性提升的底层逻辑,团队还进行了分子动力学(MD)模拟和分子对接分析。


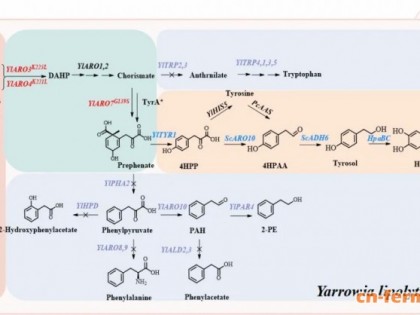
2. 代谢工程重构莽草酸途径(提升芳香前体)
为了提供充足的前体(对羟基苯甲醇, pHBAL),团队对莽草酸途径进行了系统性重配。他们对关键基因(如 aroG, aroF, aroL, talB, tktA, ppsA 以及抗反馈抑制的 ubiC)进行了不同组合的过表达测试。通过精细调控前体PEP和E4P的供应,构建了最优组合菌株,成功将发酵摇瓶中的天麻素产量推升至1.54 g/L。

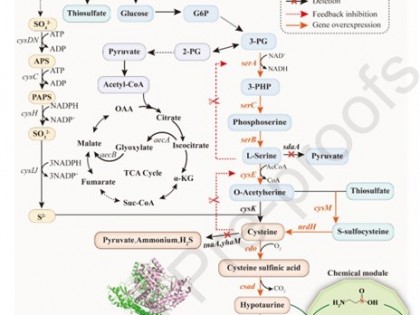
3. 构建独立的UDPG再生途径
为了解决糖基供体UDPG的供应瓶颈,团队引入了蔗糖磷酸化酶(Basp)系统(cscB-Basp-UgpA)。该系统利用蔗糖裂解直接生成1-磷酸葡萄糖(G1P)用于合成UDPG,而释放的果糖则用于细胞生长。这一策略巧妙地避免了产物合成与细胞生长的碳源竞争。

4. 1.1-L生物反应器发酵优化
在完成菌株GA02的构建后,团队将其转移到1.1升生物反应器中进行放大培养。通过严格控制发酵过程中的溶氧(DO)水平,探索细胞增殖与产物合成的最佳平衡点。

研究结论与创新点
1. 创制了高效的突变酶,揭示了催化增强机制
筛选出的三突变体 AtUGT(T282S/A294E/V463L) 催化生成天麻素的效率比野生型提高了 74.84%。分子动力学模拟表明,突变并没有改变酶与底物的亲和力,而是通过缩小底物氧原子与催化位点(His19)之间的距离,优化了催化口袋的空间几何结构,从而大幅提升了催化转换数(kcat)。
2. 实现了代谢流的完美平衡
研究发现,传统广泛使用的 ppsA(磷酸烯醇丙酮酸合成酶)过表达策略在本体系中反而会抑制产物合成和细胞生长。通过重新排布 aroF-tktA 和 aroG-aroL 基因盒,配合蔗糖磷酸化UDP-葡萄糖再生模块,实现了前体供应与辅因子再生的双重解脱,在摇瓶水平就达到了 2.18 g/L 的产量。
3. 刷新了大肠杆菌合成天麻素的纪录
在1.1-L反应器的补料分批发酵中,研究发现高溶氧(40%)会导致细胞过度生长而降低比生产率。将溶氧水平控制在 20% 时,细胞生长和产物合成达到了最佳平衡。最终在96小时的发酵后,天麻素滴度达到了惊人的 13.73 g/L。这不仅是目前大肠杆菌底盘中的最高纪录,也为糖基化芳香族化合物的绿色工业化制造提供了极具竞争力的平台。